










parallele Seiten:
|
Physik, 13 Atomphysik - Frank
Hertz Versuch |
Übersicht
| Das Experiment, das Franck und Hertz im Jahr 1914 durchführten,
ist eines der Schlüsselexperimente, die bei der Entwicklung der
modernen Atomphysik halfen. Es hat uns gezeigt, dass die Atome
Energien nur in bestimmten Portionen oder 'Quanten' aufnehmen und
bestätigte so die bohrschen Postulate. |
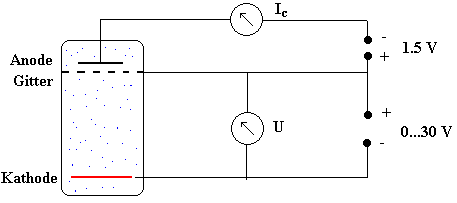 In dieser Abbildung sieht man die Umrisse einer Röhre mit der das
Experiment durchgeführt wird und die Quecksilberdampf unter
niedrigem Druck enthält. Die Glühkathode sendet Elektronen aus,
deren kinetische Energie zu Beginn praktisch 0 ist. Sie gewinnen
dadurch kinetische Energie, dass sie von einer Spannung zwischen der
Kathode und dem Gitter beschleunigt werden. |
Auf diesem Weg stoßen sie mit den Quecksilberatomen zusammen und
können dabei an Energie verlieren.
Elektronen, die eine kinetische Energie von mindestens 1,5 eV haben
wenn sie das Gitter erreichen, überwinden das Gegenfeld und gelangen zur Anode und tragen
somit zum
Anodenstrom Ic bei.
Elektronen, die beim Erreichen des Gitters weniger als 1,5 eV an
kinetischer Energie haben, können die Gegenspannung nicht
durchlaufen und tragen daher auch zum
Anodenstrom Ic nichts bei. |
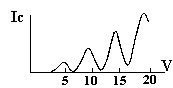 Die Stromstärke Ic zeigt mehrere
Rückgänge jeweils im Abstand von etwa 4.9 eV.
Der erste Rückgang stammt von den Elektronen, die
ihre gesamte kinetische Energie bei einem Stoß mit
einem Quecksilberatom abgegeben haben.
Der zweite Rückgang stammt von den Elektronen, die
ihre Energie bei zwei aufeinander folgenden Stößen
an zwei verschiedene Quecksilberatome abgegeben haben.
|
Java Applet
| In dem aus Spanien stammenden Applet wird der Anodenstrom Ic in
Abhängigkeit der Beschleunigungsspannung (ddp catodo-rejilla)
simmuliert. Die Messung wird durch drücken von Start (Nuevo)
gestartet. Aus der Glühkathode treten in Wirklichkeit fortlaufend
Elektronen aus. Graphisch dargestellt wird in diesem Applet nur die
vorderste Front. Reicht die Energie für eine Anregung der
Quecksilberatome, so leuchten diese rot auf. |
|
|
|
Durch drücken von
Enviar werden die Messdaten an das Diagramm Applet unten
übergeben.
Borrar löscht die
Daten (in beiden Applets). |
|
©
Ángel Franco García -1998-2005. |
| Nachdem die Messdaten durch drücken von Enviar übertragen worden
sind , können sie mit Grafica im Diagramm dargstellt werden.
Erstellt eine Messreihe von 1V-20V:
1) Tippe den entsprechenden Wert in die Box (ddp
catodo-rejilla) ein und starte mit Nuevo. Achte auf die nun links
erscheinenden schwarzen Punkte (Elektronen). Falls diese bei Stößen
das Quecksilber zum leuchten bringen färben sich diese Atome rot (wo
liegen sie). Was passiert mit den Elektronen im Gegenfeld? Übergib
den Messwert mit Enviar an das Diagramm. Fahre mit der nächsten
Spannung fort.
2) Erstelle ein Versuchsprotokoll (Hinweis für den 22.2.11: damit
haben wir schon angefangen!) mit Aufbau und Diagramm. Übertrage
außerdem für eine Spannung von 17V eine Zeichnung bei der die zum
Leuchten angeregten Atome zu sehen sind.
3) Formuliere eine Erklärung zum Frank Hertz Versuch mit eigenen
Worten. |
Erklärungen
 Bis zum 1. Maximum (»
0-5 V): Bis zum 1. Maximum (»
0-5 V):
Mit zunehmender Beschleunigungsspannung UB gelangen pro
Zeiteinheit immer mehr Elektronen zum Anode. Die Energie reicht
jedoch nicht aus, die Hg-Atome auf ein höheres Energieniveau zu
heben, es finden nur elastische Stöße statt. |
 Zwischen 1. Maximum und 1.
Minimum (» 5-6 V): Zwischen 1. Maximum und 1.
Minimum (» 5-6 V):
Die Elektronen besitzen kurz vor dem Gitter nun genügend Energie, um
die Hg-Atome anzuregen. Nun stoßen die Elektronen mit Hg-Atomen zusammenstoßen
und geben fast ihre gesamte Energie ab. Sie sind deshalb nicht mehr in der Lage, die Anode zu
erreichen. |
 Zwischen 1. Minimum und 2.
Maximum (» 6-10 V): Zwischen 1. Minimum und 2.
Maximum (» 6-10 V):
In diesem Bereich nimmt der Anodenstrom wieder zu. Die Elektronen
nehmen nun nach dem Stoß
wieder Energie im E-Feld auf (reicht nicht für eine weitere
Anregung)
und überwinden das Gegenfeld. |
 Zwischen 2. Maximum und 2.
Minimum (» 10-11 V): Zwischen 2. Maximum und 2.
Minimum (» 10-11 V):
Einige Elektronen besitzen nun vor der Anode bereits genug Energie,
um ein zwei Hg-Atom anzuregen. Der zweite Stoß findet kurz vor den Anode statt, der erste
zwischen Kathode und Anode. |
 Zwischen 2. Minimum und 3.
Maximum (» 11-15 V): Zwischen 2. Minimum und 3.
Maximum (» 11-15 V):
Die Elektronen besitzen nun nach den ersten beiden unelastischen
Stößen wieder genügend Energie, um die Anode zu
erreichen. Für einen weiteren unelastischen Stoß reicht die Energie
jedoch nicht aus. |
 Zwischen 3. Maximum und 3.
Minimum (» 15-16 V): Zwischen 3. Maximum und 3.
Minimum (» 15-16 V):
Der Strom nimmt wieder ab, was auf einen dritten unelastischen Stoß
und damit auch auf eine weitere Anregung der Atome hinweist. |
letzte Änderung: 21.2.2011 |



















